Les champignons, les plantes et les microorganismes produisent une énorme variété de composés chimiques qui ne sont pas essentiels à leur survie – les métabolites secondaires. Bien qu’il ait été démontré pour certains qu’ils fonctionnaient comme des antibiotiques, des répulsifs ou des phéromones, la fonction de la plupart de ces substances n’est pas claire. Afin de mieux comprendre le métabolisme secondaire et d’ouvrir l’accès à de nouvelles substances actives, il est nécessaire d’étudier les voies métaboliques sous-jacentes.
Au cours du siècle dernier, les expériences de marquage isotopique ont montré que les métabolites secondaires ne sont composés que d'un nombre limité d'éléments constitutifs (souvent acétate, acides aminés, isoprène ou shikimate), qui sont ensuite modifiés de diverses manières. La nature joue donc au lego chimique en combinant de manière modulaire un nombre limité de briques de base, créant ainsi un répertoire d'une grande diversité chimique. Comprendre les processus biosynthétiques qui génèrent cette diversité est donc d’une importance clé. La recherche au laboratoire d’ALUF-Medpharm (Université de Fribourg, Institut pharmaceutique, Pr Michael Müller) vise à élucider les étapes de la biosynthèse qui sont difficiles à réaliser par des méthodes chimiques classiques. Une attention particulière est accordée à la création de la diversité métabolique et, par conséquent, à l’exploration biocatalytique de classes entières de composés.
Ceci est illustré par le couplage oxydatif enzymatique des groupes phénoliques, où des monomères identiques peuvent donner naissance à des dimères différents (Fig. 1). A l'aube du nouveau millénaire, les enzymes sous-jacentes étaient pour la plupart inconnues. Grâce aux méthodes d'analyse du génome, nous sommes parvenus, ainsi que d’autres groupes, à identifier et (partiellement) décrire un certain nombre d’enzymes coupleurs du phénol.
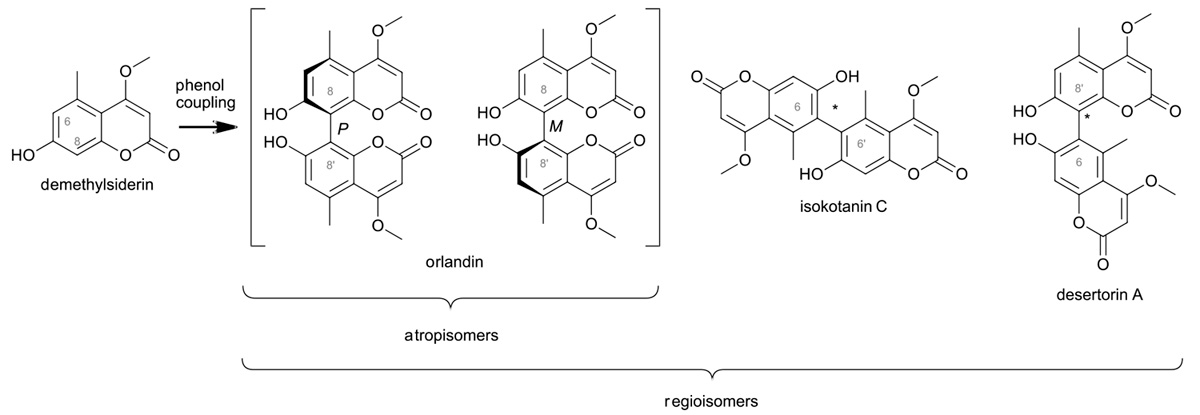
Fig. 1: le couplage oxydatif enzymatique des groupes phénoliques
Cela a montré que le couplage phénolique peut être catalysé par différents systèmes d’oxydation, en particulier des enzymes à cytochrome-P450 et des laccases, mais aussi par des peroxydases et éventuellement par des oxydases flavine-dépendantes. Alors que certaines de ces enzymes sont strictement spécifiques au substrat, d’autres (de structure très voisines) montrent un spectre plus large et acceptent plusieurs substrats. Le choix réactionnel dépendra d'une part de la présence de protéines supplémentaires, ou encore des conditions environnementales de la réaction.
Dans ce contexte, nous tenterons, dans le cadre de ce projet, d’identifier les molécules responsables à partir d’extraits fongiques bioactifs par fractionnement guidé par activité et, par la suite, d’élucider les structures des composés responsables. Les oxydoréductases dépendantes du NADPH, responsables de la synthèse des polykétides, un groupe central de métabolites secondaires fongiques, présentent un intérêt particulier.
Ces composés ciblés ou leurs variantes produites par le « lego » chimique décrit ci-dessus seront générés par synthèse chimique ou hémi-synthèse, pour obtenir suffisamment de matériel nécessaire aux tests fonctionnels. De plus, il est également possible de combiner cette modularité au niveau de la synthèse moléculaire avec la modularité du système de puces, c’est-à-dire de reconstituer les voies de réaction chimique d’intérêt sur une plate-forme microfluidique.
Publication
L. Fürtges, S. Obermaier, W. Thiele, S. Foegen and M. Müller, Diversity in Fungal Intermolecular Phenol Coupling of Polyketides – Regioselective Laccase‐based systems. ChemBioChem, 2019, 20, 1928–1932. doi.org/10.1002/cbic.201900041.
S. Obermaier and M. Müller, Biaryl-Forming Enzymes from Aspergilli Exhibit Substrate-Dependent Stereoselectivity, Biochemistry, 2019, 58, 2589–2593. doi.org/10.1002/chem.201705998
S. Obermaier, W. Thiele, L. Fürtges and M. Müller, Enantioselective Phenol Coupling by Laccases in the Biosynthesis of Fungal Dimeric Naphthopyrones. Angew. Chem. 2019, 58, 9125–9128. doi.org/10.1002/anie.201903759.
